Biodentine™: meer dan dentine in een capsule
Als cariës, trauma of slijtage tot verlies van tandweefsel leiden, wordt dit vaak vervangen door een inert dentaal vulmateriaal dat in bulk wordt aangebracht. Voor een succesvol klinisch resultaat is de materiaalkeuze doorslaggevend. De beschikbare hydrocalciumsilicaatcementen variëren onderling sterk. De clinicus moet dus voor elke behandeling de juiste optie kiezen. Ontdek hier de verschillende klinische toepassingen van Biodentine™ (Septodont), door prof. J. Camilleri.
De studie van prof. J. Camilleri
Tandweefsel gaat verloren door cariës, trauma of slijtage en wordt dikwijls vervangen door een inert dentaal vulmateriaal dat in bulk wordt aangebracht. Als de gezondheid van de pulpa in het gedrang komt moet men een aantal interventies overwegen. In eerste instantie moet men de vitaliteit van de pulpa trach ten te bewaren. In een verder stadium is men verplicht om, na het verwijderen van de infectie, de ont stane pulpa ruimte op te vullen. Bij een pulpaire verwikkeling dient men een andere benadering te vol gen en zijn materialen die een interactie aan gaan met de pulpa of de dentine geïndiceerd. Interactieve dentale materialen bevatten verschillende vormen van calciumhydroxide en meer recentelijk, hydrofiele calciumsilicaatcementen. De hydro calciumsilicaatcementen bieden als grote voor deel hun hydrofiele karakter, zodat men deze materialen kan gebruiken in een vochtige omgeving zonder gevaar voor desintegratie. Deze cementen zijn dus geschikt voor apicale vulling en het herstel van perforaties. Een andere belangrijke eigenschap bestaat in het vrijgeven van calciumhydroxide als bijproduct van de hydratatie-reactie. Dit maakt hen uitermate geschikt voor pulpa-overkapping, apexificatie en apexogenese, en recentelijk ook voor regeneratieve endodontische toepassingen. Het cal- ciumhydroxide creëert een omgeving waarin calcium ionen worden vrijgegeven en waar de antibacteriële activiteit hoog is. Voor een succesvol klinisch resultaat is de materiaalkeuze uiterst belangrijk. Zoals aangetoond in Tabel 1 zijn er een aantal hydro calciumsilicaatcementen voor verschillende toepassingen beschikbaar. Deze materialen variëren onderling in ruime mate, en de clinicus moet dus voor elke behandeling de juiste optie kiezen. In dit artikel brengen we de verschillende klinische toepassingen van Biodentine™ (Septodont, Saint-Maur-des-Fossés) onder de aandacht.
Eigenschappen van Biodentine™
Biodentine™ wordt aangeboden in een poeder/vloei – stof verpakking. Het poeder bevindt zich in een cap – sule en de vloeistof in een flacon (Fig. 1). Het poeder bevat tricalciumsilicaat, zirkoniumoxide, calciumcarbonaat en een kleine concentratie ijzeroxide voor de radiopaciteit. De vloeistof is een waterige oplossing die calciumchloride en een wateroplosbaar polymeer be vat. Biodentine™ poeder en zijn gehydrateerde producten werden duidelijk gekarakteriseerd. Het Biodentine™ ontwerp verzekert optimale eigenschappen en dus een uitstekende klinische performantie. Het poeder is fijner dan elk ander cement – type in deze categorie (Tabel 2), met een hoger reactie vermogen als gevolg. Het poeder bevat vooral tricalciumsilicaat (Tabel 3) in tegenstelling tot de andere watergebaseerde cementen die voornamelijk bestaan uit Portland cement, zoals blijkt uit Tabel 1. Het zuivere tricalciumsilicaat bevat geen alumi – nium (1,2) en metaalsporen (3) zoals die aanwezig zijn in de producten op basis van Portlandcement. In tegenstelling tot de materialen die bismutoxide als opaker gebruiken, geeft zirkoniumoxide een adequate en stabiele radio-opaciteit zonder risico op lekkage en verkleuring (4-6). De RX-diffractie analyse laat duidelijk de voornaamste bestanddelen zien van het Biodentine™ poeder (Fig. 2). Ter verbetering van de eigenschappen bevat Biodentine™ additieven waaronder calciumcarbonaat in het poeder, calciumchloride en wateroplosbaar polymeer in de vloeistof. Het calciumcarbonaat zorgt, na het mengen van poeder en vloeistof tot een oplossing, voor een bron van vrije calciumionen. Deze zorgen voor een vroegtijdige warmte-
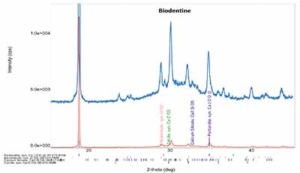
Fig. 2: RX-diffractie analyse van Biodentine™ poeder om de voornaamste bestanddelen aan te tonen, met name: tricalciumsilicaat, zirkoniumoxide en calciumcarbonaat. Met toestemming van Camilleri et al. 2013.
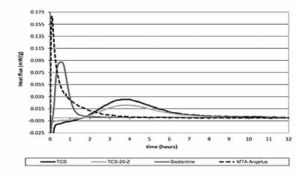
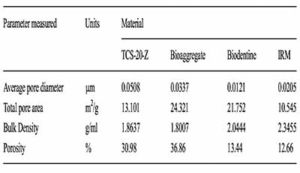
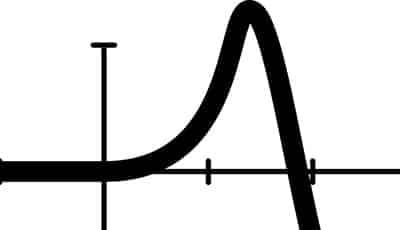
ontwikkeling tijdens de reactie, waardoor deze inten- siever gaat verlopen, zoals aangetoond in Fig. 3. Calciumchloride vermindert de uithardingstijd van Biodentine™ aanzienlijk in vergelijking met andere ge – lijkaardige materialen (7,8). Het wateroplosbaar poly – meer vermindert het waterige aandeel in de cement wat de fysische eigenschappen van Biodentine™ ten goede komt. Inderdaad, de druksterkte en micro- hardheid van Biodentine™ zijn beduidend hoger dan deze in andere vergelijkbare cementen (7). De microstructuur van Biodentine™ (Fig. 4) toont hoe door de hydratatie het tricalciumsilicaat reageert en rond de calciumcarbonaat partikels neerslaat (9). Er wordt een grote hoeveelheid calciumhydroxide geproduceerd, zoals aangetoond op de RX-diffractie scan van de gehydrateerde materialen (10). Men ziet een duidelijke piek bij 18 graden (Fig. 5). De specifieke chemische samenstelling, de kleine partikelgrootte, de lage waterconcentratie en de aanwezigheid van calciumcarbonaat dragen allemaal bij tot de optimale materiaaleigenschappen die nodig zijn voor een klinische performantie. Bovendien is het materiaal weinig poreus (Tabel 4) in vergelijking met de andere materialen (11), wat ook een klinisch voordeel oplevert. Vermits het een watergebaseerd materiaal is mag men het niet laten uitdrogen, wat zou leiden tot scheuren ter hoogte van de interface (Fig. 6) en in het materiaal zelf (11).
Fig. 3: Uitgesproken warmteontwikkeling in Biodentine™ vroeg in de hydratatie-reactie. (TCS: Tricalciumsilicaatcement; TCS-20-Z is een tricalciumsilicaatcement met 20% zirkoniumoxide). Met toestemming van Camilleri et al. 2013.
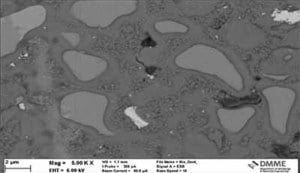
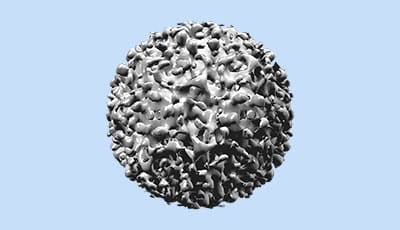
Fig. 4: Electromicrografische scan van de Biodentine™ reactie toont de microstructuur. Met toestemming van Camilleri et al. 2013.
Fig. 5: RX-diffractie kaart van de Biodentine™ reactie toont de voornaamste fases na de reactievorming. Calciumhydroxide overheerst. Met toestemming van Camilleri et al. 2014.
Fig. 6: De confocale laser microscopie van Biodentine™ in droge en natte HBSS ( Hanks Balanced Salt Solution) omgeving bevestigt dat men het product altijd vochtig moet houden. Met toestemming van Camilleri et al. 2014.
Tabel 4: Percentage porositeit in Biodentine™ vergeleken met gelijkaardige materialen. Met toestemming van Camilleri et al. 2014.
—
Meer informatie of praktijkdemonstratie
Vraag meer informatie of uw praktijkdemonstratie aan via info@septodont.nl of tel. 0800 2 425 60 37.
—
Klinische toepassingen
Pulpakapping en dentine vervanging
Biodentine™ stelt calciumionen vrij (10,12) in een hogere concentratie dan andere vergelijkbare materialen (12,13), dus is het een ideaal overkappingsmateriaal. Het Biodentine™ oppervlak vertoont de dikste calciumlaag vergeleken met ProRoot MTA, Dycal en Theracal (14). Bij een directe pulpakapping met Biodentine™ zien we klinisch een duidelijke dentinebrug (15,16,17). Bij klinische gevallen waarbij een irreversibele pulpitis behandeld werd met Biodentine™ constateren we met een Cone Beam op – name (18) een reductie van de ontsteking ter hoogte van de apicale regio. De pulpaire reactie op Biodentine™ kan men vergelijken met andere gelijkaardige materialen zoals mineraal trioxide aggre – gaat (19), met celproliferatie en alkalinefosfaat activiteit uitgaande van humane dentale pulpacellen (20). Men nam dezelfde reactie waar bij testen met Biodentine™ percolaat (13). Het vrijstellen van calcium draagt ook bij tot de belangrijke antimicrobiële eigen schappen, omdat dentale cariës immers een bacterieel gebaseerde ziekte is. Biodentine™ bezit lagere antimicrobiële eigenschappen (13) dan calciumhydroxide overkappingsmaterialen, maar deze materialen vertonen een hogere cytotoxiciteit (21).
Door zijn fysische kwaliteit kan men dit materiaal bovendien in bulk gebruiken zonder te moeten layeren, waardoor het risico op randlekkage en bij komend falen van de restauratie vermindert. Biodentine™ toont inderdaad minder microlekkage dan kunsthars gebaseerde vulmaterialen (22). Het plaatsen van een definitieve restauratie over het watergebaseerde Biodentine™ betekent een uitdaging. Men stelt dit best minstens 2 weken uit, waarbij men zowel de total-etch als self-etch techniek kan gebruiken (23). De total-etch techniek kan tot microstructurele veranderingen (24) in het materiaal leiden, maar hoewel het verlies van alle in vitro geplaatste composiet restauraties te wijten was aan de thermocyclus, bleek total-etch toch efficiënter dan self-etch (25). Fig.7 toont de micro – structuur en interface van Biodentine™ en composiet bij gebruik van total-etch en self-etch adhesieven. Men kan Biodentine™ tot 6 maanden als basis vulmateriaal gebruiken, waarna men het overkapt met een composiet en zo een doeltreffend dentine vervangend materiaal verkrijgt (26).
Andere tricalciumsilicaatmaterialen voor pulpakapping die kunsthars bevatten bieden het voor deel dat ze kunnen gelayerd worden met het composiet restauratiemateriaal, en zo een sterke binding tot stand brengen (25). Hun effect op de pulpa is echter minderwaardig (27). De vrijstelling van calciumionen door deze materialen is laag en er wordt geen kristallijne calciumhydroxidelaag gevormd (10). De penetratie en hydratatie van de actieve component tricalciumsilicaat in kunsthars gebaseerde
Fig. 7: Micro-structuur en interface van Biodentine™ en composiet bij gebruik van total-etch en self-etch adhesieven. Met toestemming van Meraji en Camilleri et al. 2017
overkappingsmaterialen zoals Theracal, hangt af van de omgevende vochtigheid. Deze vochtpenetratie is onvoldoende zoals een model met geëxtraheerde tanden die 15 dagen in een medium werden bewaard, aantoont (28). In overeenstemming met vroeger onderzoek bevestigen in-vitro (29) en in-vivo (30) studies dat Theracal-geconditioneerde media beduidend minder proliferatie van pulpa- fibroblasten vertoonden, en dat ze bij in cultuur gebrachte pulpa-fibroblasten en volledige tanden de vrijstelling van pro-inflammatoire interleukine 8 induceerden.
Het volledige tandcultuur model (31) en een recente klinische studie (30) volgend, is het duidelijk dat Bio – dentine™ betere biologische en klinische eigen- schappen bezit dan de kunsthars gebaseerde materialen. Biodentine™ blijkt in alle gevallen het meest geschikt om in te staan voor een volledige genezing van de pulpa (30).
Pulpotomieën
Vooral bij melktanden zal een diepere beschadiging van de pulpa uitmonden in pulpotomie-procedures. In contact met stamcellen uit humane melk – tandfollikels toont Biodentine™ een hogere cytocompabiliteit en bio-activiteit dan MTA Angelus, Theracal en IRM (32). Op een dierlijk model waarbij men Biodentine™ als pulpotomie-agens gebruikte, zag men in vergelijking met MTA een dikkere gemineraliseerde weefselbrug, die ook veel gemakkelijker op radiografie te detecteren viel (33).
Het klinische succes van Biodentine™ bij pulpotomie op melkmolaren ligt veel hoger dan de stan – daard procedures met formocresol (34,35). Biodentine™ en calciumhydroxide tonen hetzelfde regeneratieve potentieel en activiteit, behalve de fysische en klinische beperkingen van dit laatste (36). Pulpotomieën die uitgevoerd werden met Biodentine™ vertoonden hetzelfde voorspelbaar klinische resultaat als die met MTA (37-41), en waarderen hoger dan de minder courante behandelingen met laser (41) en propolis (39). Biodentine™ geeft ook geen verkleuring van de behandelde gebitselementen (42).
Behandeling van de onvolgroeide apex
Het verlies van pulpaweefsel vergt een wortel kanaalvulling. Onvolgroeide tanden stellen hierbij een anatomisch probleem vanwege de korte en dunne wortels waardoor een breuk niet ondenkbaar is. Door de specifieke configuratie van het wortelkanaal is een kanaalvulling dan ook een uitdaging.
Een apexificatie behandeling bestaat in het afsluiten van de apex ten opzichte van de peri-apicale ruimte door het vormen van een gecalcificeerde barrière. Hiervoor creëert men een omgeving waar – bij calciumionen uit de omgevende dentine worden vrijgesteld om een calciumbrug te vormen. Men doet dit met materialen die calciumhydroxide afgeven waarbij de veelgebruikte, oplosbare calciumhydroxide pasta’s. Dit calciumhydroxide stelt de nodige calciumionen vrij om een ideale omgeving voor de brugvorming te creëren (43). Deze pasta’s bieden het bijkomend voordeel dat ze een anti bacteriële werking hebben, vermits het meestal gaat om genecroseerde elementen die ten prooi vielen aan bacteriële invasies (44). De behandeling met deze oplosbare pasta’s moet in verschillende zittijden verspreid over een aantal maanden uitgevoerd worden, en de gevormde calciumbrug blijkt vrij poreus te zijn (45).
Het sluiten van de apex met een hydro calciumsilicaat plug kan in twee zittijden uitgevoerd worden. Dit was nodig omdat MTA een lange uithardingstijd heeft en men pas dan de definitieve vulling kan plaatsen. Recentelijk toonde men echter aan dat dezelfde behandeling met Biodentine™ slechts één zittijd behoeft omdat vocht geen invloed heeft op de eigenschappen van dit materiaal (46).
Zo krijgt men een voorspelbaar resultaat en een alternatief voor het gebruik van calciumhydroxide (47). Door hun hydrofiele karakter en de vorming van calciumhydroxide zijn dit ideale materialen voor deze behandelingen. Biodentine™ stelt meer calciumionen vrij dan MTA (2) en is uiterst succesvol als apicale plug bij apexificatie (48-53). De toevoeging van calciumcarbonaat geeft de reactie in het begin – stadium een boost, met een optimale hydra tatie als resultaat. De toevoeging van calciumchloride accelerator en het wateroplosbaar polymeer zorgt voor een lage water/poeder verhouding (2). Er worden geen pozzolanen of andere cementsubstanties aan toegevoegd, zoals blijkt uit Tabel 1. Men stelde vast dat deze materialen de calciumhydroxide vorming afremden (54,55). De breukweerstand van onvolgroeide tanden met een apicale Biodentine™ plug blijkt dezelfde als die van MTA, maar hoger dan de controlegroep (52).
Biodentine™ werd ook succesvol gebruikt bij rege- neratieve endodontie (56-58). Ook hier was de breuk- weerstand identiek aan die van MTA (59), maar met de minste verkleuring (60); dus het keuzemateriaal bij regeneratieve endo, vooral waar esthetiek belangrijk is.
Apicale vulling en herstelling van perforaties
Apicale vulcementen dienen aan specifieke eisen te voldoen omdat ze hun klinisch succes moeten bewijzen in zeer ongunstige omstandigheden. Het hydrofiele karakter van tricalciumsilicaat lijkt dus een belangrijk pluspunt. Men ontwikkelde deze materialen dan ook voor dit specifieke doel. Hydrofiele cementen hebben de eigenschap te reageren met de omgeving waarin ze geplaatst worden, en apicaalwaarts komen ze in contact met bloed.
Maar ze staan eveneens in contact met de wortel – dentine, guttapercha-en sealer resten die gebruikt werden voor de kanaalvulling. Weefselvocht en bloed hebben geen effect op de fysische eigenschappen van Biodentine™ (61), en bovendien bindt het sterker dan MTA. Beide materialen kunnen noch – tans door bloed gecontamineerd worden (62). Men vond minder bacteriën in een apicale regio behandeld met Biodentine™ ten opzichte van MTA (63), wat bewijst dat Biodentine™ een sterker antimicrobiële vermogen heeft. Ook de biocompabiliteit van Biodentine™ ligt hoger dan die van MTA, met een betere celadhesie bij gebruik als apicaal vulmateriaal (64). Ook voor het herstellen van perforaties lijkt Biodentine™ uitermate geschikt (65), omdat het een positieve weefselreactie en een minerale afzetting uitlokt ter hoogte van de perforatiesite. Deze reactie is te wijten aan de vrijstelling van opgeloste calciumhydroxide ionen. Ook sluit Biodentine™ het defect hermetisch af, wat noodzakelijk is in een zone die toch altijd sterk geïnfecteerd is.
Materialen voor het herstellen van een perforatie kunnen ook loskomen tijdens de verdere restauratie van het element. Biodentine™ toont een sterke initiële binding tegen trekspanning die niet verloren gaat in contact met bloed (68). Bovendien wordt het niet beïnvloed door irrigatiemiddelen (69), wat duidt op stabiliteit.
Besluit
Biodentine™ is een tweede generatie hydro calciumsilicaatmateriaal dat vooral samengesteld is uit tricalciumsilicaat, aangevuld met zirko niumoxide als opaker en enkele andere additieven. Het werd wetenschappelijk ontworpen met als specifieke doelstelling om gebruikt te worden als een den tine vervangmateriaal. Dit wordt bevestigd door de bestaande onderzoeken, maar ook andere klinische toepassingen bieden zich aan. Het is dus zeker meer dan dentine in een capsule.
Meer informatie of praktijkdemonstratie
Vraag meer informatie of uw praktijkdemonstratie aan via info@septodont.nl of tel. 0800 2 425 60 37.
Door: Josette Camilleri B.Ch.D., M.Phil., Ph.D., FICD, FADM, FIMMM, FHEA (UK) School of Dentistry, Institute of Clinical Sciences College of Medical and Dental Sciences The University of Birmingham Birmingham U.K.
Professor Josette Camilleri obtained her Bachelor of Dental Surgery and Master of Philosophy in Dental Surgery from the University of Malta. She completed her doctoral degree, supervised by the late Professor Tom Pitt Ford, at Guy’s Hospital, King’s College London. She has worked at the Department of Civil and Structural Engineering, Faculty for the Built Environment, University of Malta and at the Department of Restorative Dentistry, Faculty of Dental Surgery, University of Malta. She is currently a senior academic at the School of Dentistry, University of Birmingham, U.K. Her research interests include endodontic materials such as root-end filling materials and root canal sealers, with particular interest in mineral trioxide aggregate, Portland cement hydration and other cementitious materials used as biomaterials and also in the construction industry. Josette has published over 100 papers in peer-reviewed international journals and her work is cited over 4000 times. She is the Editor of “Mineral trioxide aggregate. From preparation to application” published by Springer in 2014. She is a contributing author to the 7th edition of “Harty’s Endodontics in Clinical Practice” (Editor: BS Chong) and “Glass ionomer cements in Dentistry” (Editor: SK Sidhu). She is an international lecturer, a reviewer and a member of the scientific panel of a number of international journals including the Journal of Endodontics, Scientific Reports, Dental Materials, Clinical Oral Investigation, Journal of Dentistry, Acta Odontologica Scandinavica and Acta Biomaterialia.